Patrząc na strukturę rezonansową 1a , nie wydaje się, aby tropon był aromatyczny. Jednak struktura rezonansowa 1b z $ \ ce {C + -O -} $ spełnia regułę Hückela dotyczącą aromatyczności. Czy można powiedzieć, że tropon jest wtedy aromatyczny?
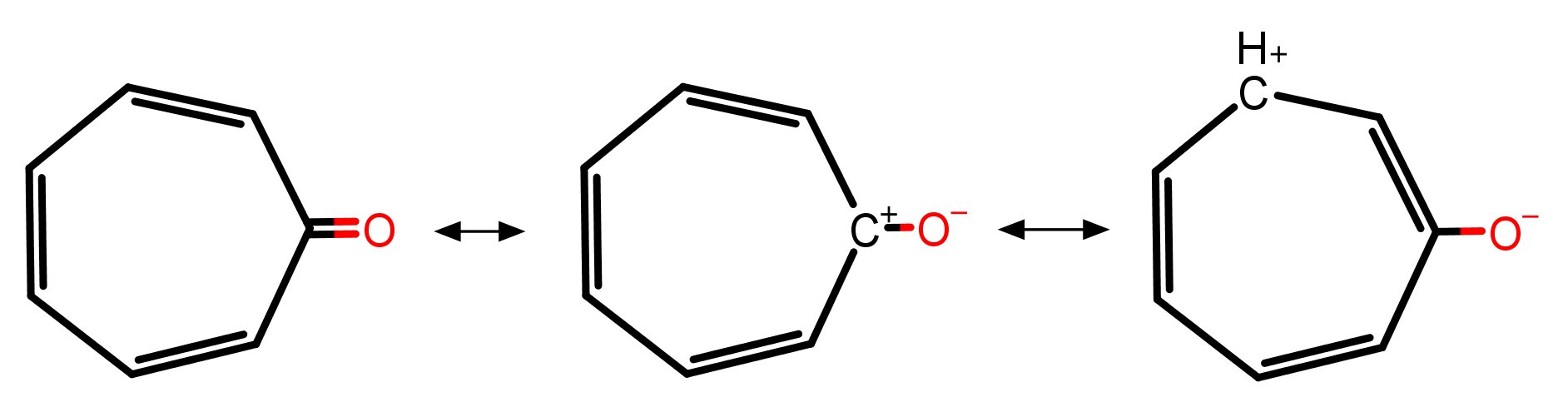
Tropon, czyli 2,4,6-cykloheptatrien-1-on, jest aromatycznym węglowodorem nie będącym benzenoidem. Jeśli spojrzysz na struktury rezonansowe na poniższym rysunku, zobaczysz, że struktura B
przedstawia cząsteczkę z ciągłą, płaską pętlą 7-orbitali p, która zawiera 6 pi-elektronów. Każdy planarny (lub prawie płaski), cykliczny układ z ciągłą pętlą p-orbitali jest uważany za aromatyczny lub stabilizowany, jeśli zawiera 4n + 2 pi-elektronów i antyaromatyczny, jeśli zawiera 4n pi-elektronów. Na tej podstawie, cząsteczki takie jak kation cyklopropenylu (4n + 2, n = 0), benzen (n = 1), kation cykloheptatrienu (tropylium) (n = 1), dianion cyklooktatetraenu (n = 2) byłyby uważane za układy aromatyczne. Odpowiednio, anion cyklopropenylowy (4n, n = 1), cyklobutadien (n = 1), kation cyklopentadienylowy (n = 1), cyklooktatetraen (jeśli była to płaska cząsteczka, n = 2) są uważane za destabilizowane lub antyaromatyczne.
Najlepszą odpowiedź na ten temat daje prawdopodobnie Barach w swojej książce
BACHRACH, Steven M. Computational organic chemistry. Raporty roczne, sekcja „B” (Chemia organiczna), 2008, 104: 394-426. str. 144
nie ma jednej definicji aromatyczności, ale raczej zbiór właściwości związanych z cząsteczkami aromatów. Właściwości te obejmują:
Związki aromatyczne są stabilne w porównaniu z niektórymi niearomatycznymi odniesieniami
Związki aromatyczne wykazują właściwości magnetyczne związane z prądem pierścieniowym. Obejmują one niezwykłe przesunięcia chemiczne, zwłaszcza protony, duże anizotropie magnetyczne i duże egzaltacje podatności diamagnetycznej.
Związki aromatyczne są zwykle płaskie i mają równoważne długości wiązań CC, mimo że formalna struktura Lewisa wskazuje na przemienne wiązania pojedyncze i podwójne wokół pierścienie.
Chociaż ich struktury kropkowe Lewisa wykazują wiązania C = C, związki aromatyczne wolą reakcję podstawienia od reakcji addycji
Zgodnie z tą definicją Tropon można uznać za aromatyczny .
Przydatne informacje znalazłem także w książce SCHERRER, Robert (red.). Środki przeciwzapalne Część II: Chemia i farmakologia. Elsevier, 2012.
tam można znaleźć, że nie było zgody co do aromatyczności troponu, ponieważ
... badanie troponu, tropolonu i ich pochodnych wydawało się w celu potwierdzenia charakteru aromatycznego, który przypisano znacznemu udziałowi struktury rezonansu dipolarnego. ... Bertelli i Andrews (1969) ponownie ocenili kwestię charakteru aromatycznego w troponie i związkach pokrewnych, korzystając z danych pochodzących z pomiarów dipolowych ... Shimanouchi i Sasaada w 1970 r. Stwierdzili, że cząsteczka jest prawie płaska. Autorzy wskazali nam, że średnia długość CC (1,407 Angrstrom) zgadzała się ze standardową wartością aromatyczną ... Deewar i Trinajstic (1970) sugerują, że związki te bardziej przypominają polienony.
Kalsi w swojej książce KALSI, P. S. Spectroscopy of Organic związki. New Age International, 2007. donosi, że tropon reprezentuje szereg struktur dipolarnych, które tworzą aromatyczny układ tropylium), a także Agrawal w swojej książce AGRAWAL, O. P. Organie chemistry reakcje i odczynniki. 1996. zgłoś, że mieszając się z wodą, wrze w 113 ° C, silnie polarny ( $ \ mu $ 4,3 D) i brakuje mu właściwości ketonowych. Ponieważ
wszystkie te właściwości można wyjaśnić na podstawie tego, że tropon jest hybrydą rezonansową trzech struktur) .. hybryda rezonansowa II troponu wskazuje również, że pierścień troponu zawiera 6 $ \ pi $ -elektrony w cyklicznym układzie rezonansowym i dlatego zachowują się jak związek aromatyczny. Pod względem chemicznym tropon zachowuje się częściowo jak związek nienasycony, a mianowicie. odbarwia wodny roztwór nadmanganianu potasu, dodaje chloru i bromu i ulega reakcji Diel'a-Aldera z bezwodnikiem maleinowym. Z drugiej strony wykazuje również charakterystykę benzenoidów, na co wskazuje tworzenie 2,4,7-tribromotroponu i 2-aminotroponu odpowiednio po bromowaniu i aminowaniu.
Więc myślę, że jest nie tylko jedna odpowiedź, ale zależy to od aspektu, na który patrzysz, ale aby podsumować
pro
-
jest prawie płaska o średniej długości CC, która jest zgodna ze standardowym aromatem
-
mieszalny w wodzie (wskazówka na interakcję z $ \ pi $ elektronów)
-
brak właściwości chetonicznych
-
stabilny ze względu na to, że jest hybryda rezonansowa 5. reaguje tworząc 2,4,7-tribromotropon i 2-aminotropon odpowiednio przez bromowanie i aminowanie
wady
- pomiary dipolowe
- odbarwić wodny roztwór nadmanganianu potasu
- dodać chlor i brom
- ulega reakcji Dielsa-Aldera z bezwodnikiem maleinowym