Znajdowanie minimum: ogólny pogląd
Minimalizując energię poszukujesz (metodami numerycznymi) minimum energii potencjalnej). Jesteś na minimum, gdy pochodna (jakobian) jest równa zero. Jest jednak kilka niestabilnych miejsc, które również mają pochodną zera, a mianowicie punkty siodełka i maksima (wierzchołek koła). Jesteśmy po minimum (na dole koła).
Pomyśl o wahadle. Ma dwa miejsca, w których pochodna wynosi zero ... kiedy jest całkowicie w górę i całkowicie w dół, ale tylko wtedy, gdy jest w skrajnej pozycji, jest stabilna. Kiedy hesjan (druga pochodna) jest określony dodatnio, jesteś na „dole wychylenia wahadła” i na minimum. Wahadło w górę pochodnej wynosi zero, ale to jest maksimum.
Jest też problem, że często w krajobrazach energetycznych wygląda jak kolejka górska ... Na prośbę komentujących lepsze zdjęcie (zaczerpnięte z wikipedii, źródło w opisie zdjęcia)
![AimNature [CC BY-SA 3.0 (https://creativecommons.org/licenses/by-sa/3.0)]](https://chemia.narkive.pl/9nuwnKEm/zdefiniuj-w-a-ciwie-zdefiniuj-stabilno-i-energi-zwi-zku:i.1.full)
Musimy znaleźć nie tylko minimum, które ma pochodną zero, ale także najniższe ze wszystkich obecnych minimów. Jest to naprawdę trudny problem, ponieważ rozwiązania numeryczne zatrzymują się, gdy pochodna wynosi zero. Nie wiedzą, że istnieją inne minimum. Istnieją metody, aby to obejść, ale jest to bardzo aktywny obszar badań i na każdego, kto może zagwarantować globalne minimum, czeka ogromna nagroda.
Myśl o energii
Czym jest ta energia, którą minimalizujemy? Minimalizujemy energię w porównaniu z punktem odniesienia. Wszystko jest zawsze w odniesieniu do punktu odniesienia.
Nie jestem chemikiem i nie znam się zbyt dobrze na mechanice kwantowej, ale spróbuję udzielić chemicznej odpowiedzi ... Takie jest moje wrażenie na temat tego, co się dzieje w scenariuszu, o który pytasz. Wykonuję minimalizacje na darmowej energii, ale to jest powiązane, ale nie do końca to, czego szukasz. W mechanice kwantowej punktem odniesienia jest moment, w którym wszystkie jądra i elektrony walencyjne są nieskończenie oddalone od siebie. Innym powszechnym punktem odniesienia w chemii, fizyce i inżynierii jest gaz idealny, w którym wszystkie cząsteczki są nieskończenie oddalone od siebie, ale atomy (i elektrony) są nadal ze sobą połączone.
Biorąc pod uwagę punkt odniesienia które określamy jako „zerową” energię, dla każdego konformera obliczylibyśmy energię potrzebną do utworzenia wszystkich wiązań kowalencyjnych w cząsteczce, czyli obliczyć energię potrzebną do przyciągnięcia elektronów walencyjnych i jąder z nieskończenie odległych miejsc i umieść je w dokładnie takiej geometrii, jaką chcesz. Zrób to dla wielu geometrii. Ten, który uformował się z najniższą energią, będzie najstabilniejszym z tych, których próbowałeś (mogą być inne, których nie próbowałeś! Możesz nadal znajdować się w niewłaściwej pętli kolejki górskiej). Rozmieszczenie dwóch jąder w różnych odległościach wymaga różnej ilości pracy itp. W praktyce programy QM robią to wszystko za nas i robią się dość szybko, ale nadal może to zająć bardzo dużo czasu. Trudno to obliczyć.
Energie wiązań
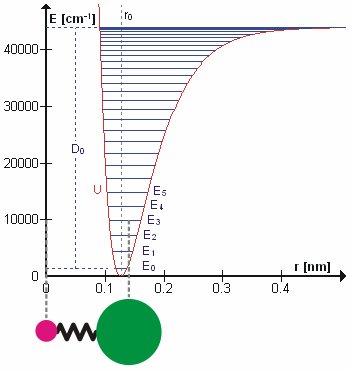
Generalnie w mechanice molekularnej energie wiązań są obliczane przy użyciu aproksymacji harmonicznej sprężyny (prawo haczyka), jednak poniższy obraz przedstawia obliczoną QM energie.
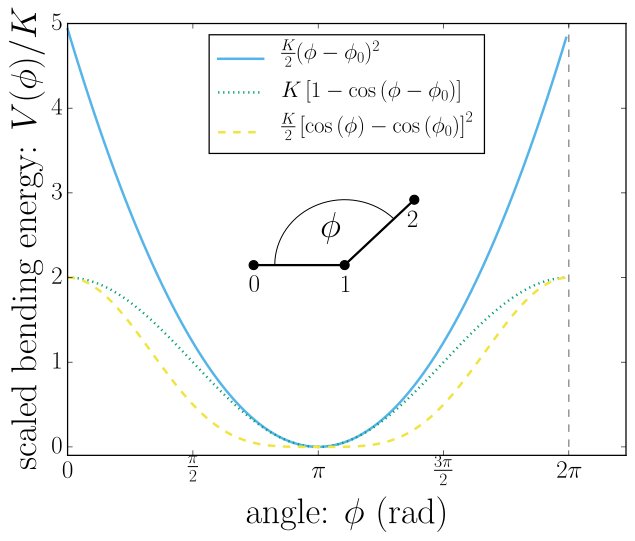
Angle Energies
Oto zdjęcie z strony internetowej programu Simualtion Espresso co pokazuje, że energia potrzebna do zgięcia kąta jest ściśle przybliżona funkcją kwadratową
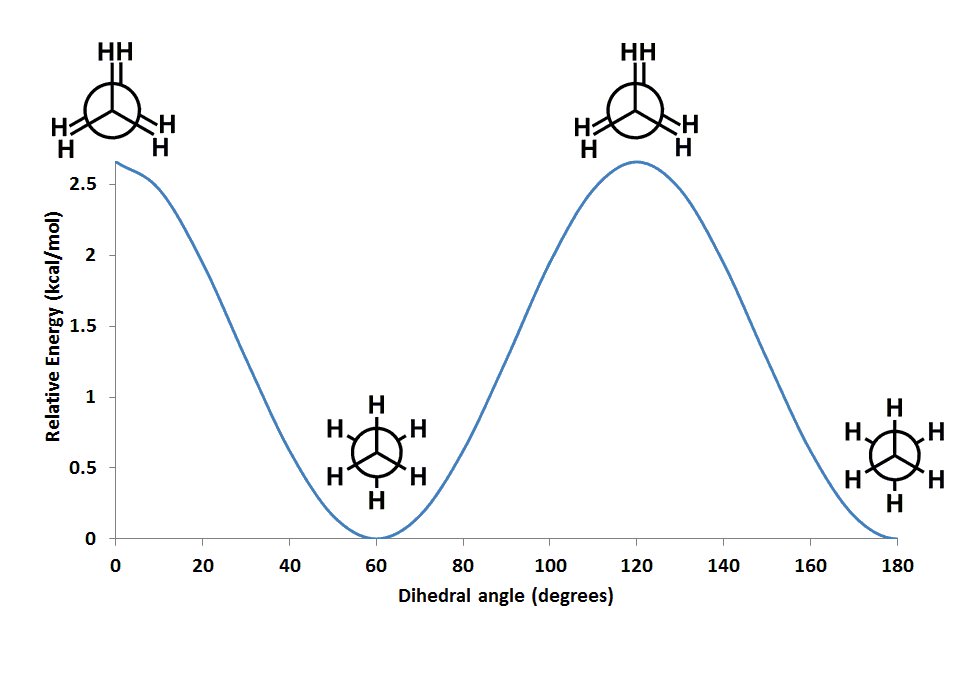
Energie skrętne
Energie skręcania są bardziej skomplikowane niż energia potencjalna wiązania i kąta, ponieważ kąt skręcenia musi być w stanie obrócić o 360 stopni i wrócić tam, gdzie się zaczął. Oto energia dla różnych konformerów, gdy obrócona zostanie geometria kąta skręcenia. Z powodu różnych geometrii jądra i elektrony znajdują się w różnych odległościach od siebie, a przeniesienie ich z nieskończenie daleko od siebie do każdej z tych geometrii wymaga różnej ilości pracy (energii). Zdjęcie pochodzi z tutaj.
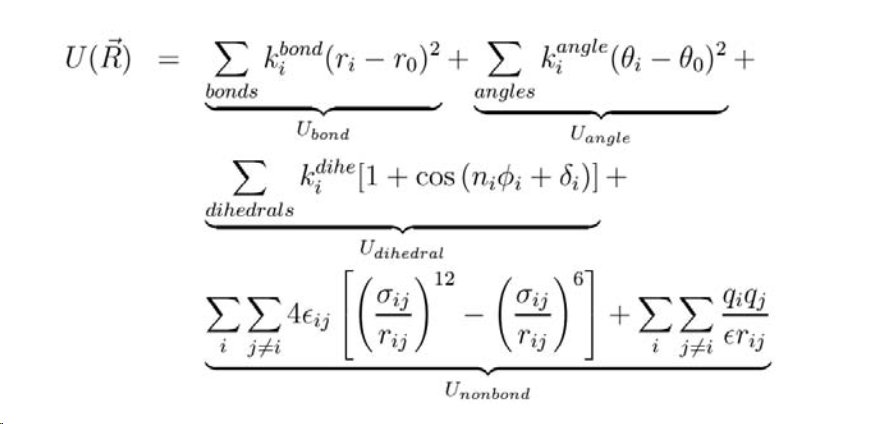
Force-Fields
W mechanice molekularnej używamy funkcji (zwanych polami sił) do przybliżenia powyższego potencjalnego wkładu energii. Oto ogólny zestaw zastosowanych równań. Możesz znaleźć minimum energii, zmieniając długości wiązań / kąty / parametry skręcania dla pojedynczej cząsteczki, a po każdej zmianie obliczając energię. Geometria z najniższą energią jest najbardziej stabilna, ponieważ cząsteczki, podobnie jak ludzie, zawsze podążają ścieżką najmniejszego oporu. Skopiowałem równania jako obraz z tutaj