Myślę, że kluczem do tego pytania jest zrozumienie różnicy między stabilnością termodynamiczną i kinetyczną. W tym poście uważam odpowiedź Thomija za najbardziej rygorystyczną i pouczającą.
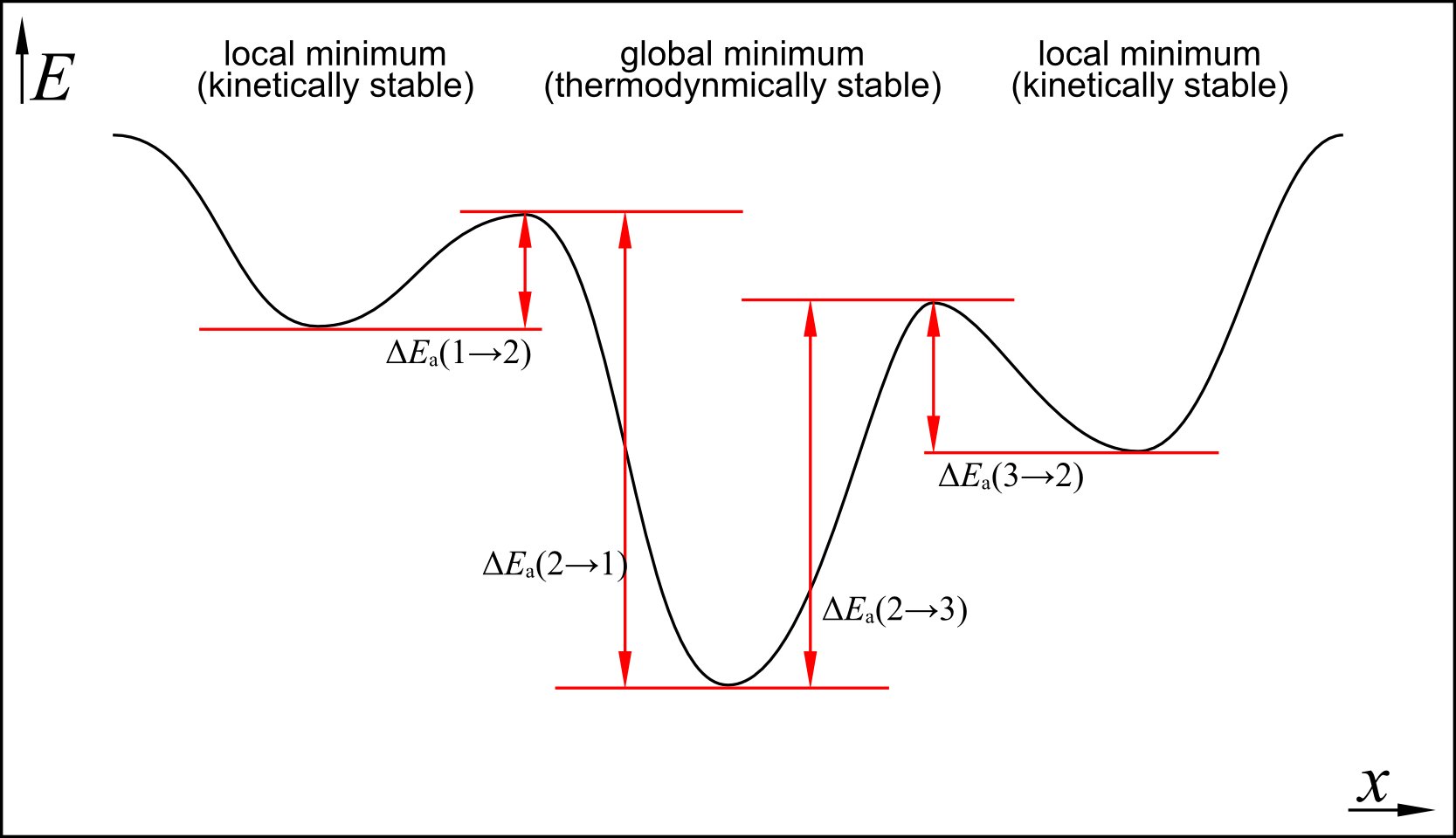
Z tego powinieneś dowiedzieć się, że termodynamicznie najbardziej stabilny alotrop odpowiada globalnemu minimum na powierzchni energii potencjalnej podczas gdy kinetycznie stabilny alotrop, tj. utrudniony przez barierę aktywacji, odpowiada lokalnemu minimum. Z tego można łatwo zauważyć, że alotrop najbardziej stabilny termodynamicznie jest również alotropem najbardziej stabilnym kinetycznie. Wynika to z faktu, że bariery wzajemnej przemiany różnych odmian alotropowych zawsze muszą być wyższe dla najbardziej stabilnej.
W poniższym dwuwymiarowym przypadku widzisz, że termodynamicznie najbardziej stabilne, tj. minimum globalne, jest otoczone dwoma lokalnymi minimami. Zawsze musi być prawdą, że $ E_ \ mathrm {a} (1 \ to2) <E_ \ mathrm {a} (2 \ to1) $, jeśli 1 $ to lokalność, a 2 $ to minimum globalne. To samo dotyczy drugiego przypadku. Gdyby to nie było prawdą, to 2 $ nie może być globalnym minimum, a zatem nie jest termodynamicznie najbardziej stabilną modyfikacją.
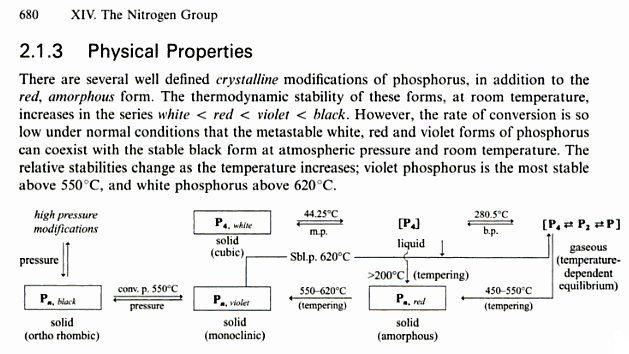
Po ustaleniu tego jest prawdą, że fosfor czarny jest formą najbardziej stabilną termodynamicznie i kinetycznie, patrz Hollemann-Wiberg, str. 680.
Jednak patrząc na inną reakcję, sprawa może nie być już taka prosta. Odnosi się to nawet do różnych temperatur, co pokaże poniższa grafika (cytat z połączonej książki).