Ponieważ $ \ mathrm {pI} $ jest $ \ mathrm {pH} $, przy którym aminokwas nie ma całkowitego ładunku netto, musisz uśrednić wartości $ \ mathrm pK_ \ mathrm a $ związane z protonacją / deprotonowanie formularza bez opłaty netto . Oto równowagi kwasowo-zasadowe dla tyrozyny:
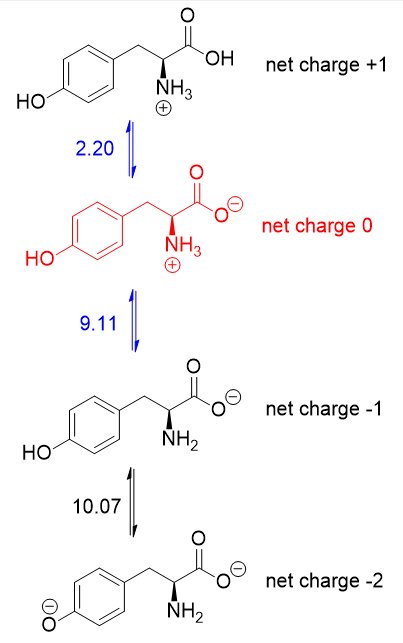
Postać bez ładunku netto jest na czerwono (+1 i -1 anuluj nie daje żadnych opłat netto). Liczy się wartość $ \ mathrm pK_ \ mathrm a $ po obu stronach tego formularza (na niebiesko), stąd $ \ mathrm {pI} $ tyrozyny wynosi 5,66 $ (średnio 2,20 $ i 9,11 $).
Tak się składa, że 2,20 $ to karboksyl $ \ mathrm pK_ \ mathrm a $, a 9,11 $ to amino $ \ mathrm pK_ \ mathrm a $. Jeśli łańcuch boczny $ \ mathrm pK_ \ mathrm a $ był niższy niż 9,11 $, to zamiast tego powinieneś uśrednić karboksyl i łańcuch boczny $ \ mathrm pK_ \ mathrm a $.
Ta sama logika ma zastosowanie do cysteiny ( wyszukaj wartości $ \ mathrm pK_ \ mathrm a $ i narysuj formy protonowane w różny sposób). Przekonasz się, że ponieważ łańcuch boczny ma niższą $ \ mathrm pK_ \ mathrm a $ niż grupa aminowa, uśredniasz karboksyl i łańcuch boczny $ \ mathrm pK_ \ mathrm a $ 's.
Ta procedura może oczywiście zostać rozszerzona na aminokwasy z kwasowymi łańcuchami bocznymi (kwas asparaginowy; kwas glutaminowy) oraz te z zasadowymi łańcuchami bocznymi (lizyna; arginina; histydyna).